Beratungsthemen in pharmazeutischer Analytik und Qualitätskontrolle

- Arzneibuch-Anforderungen und -prüfungen
- Analytische Datenintegrität, Beurteilung und kontinuierliche Verbesserung der Methoden-Leistungsfähigkeit
- Lebenszyklus-Management analytischer Verfahren,
Identifizierung und Monitoring relevanter Leistungsparameter,
Bewertung von Änderungen - Methodeneignung – und vergleich
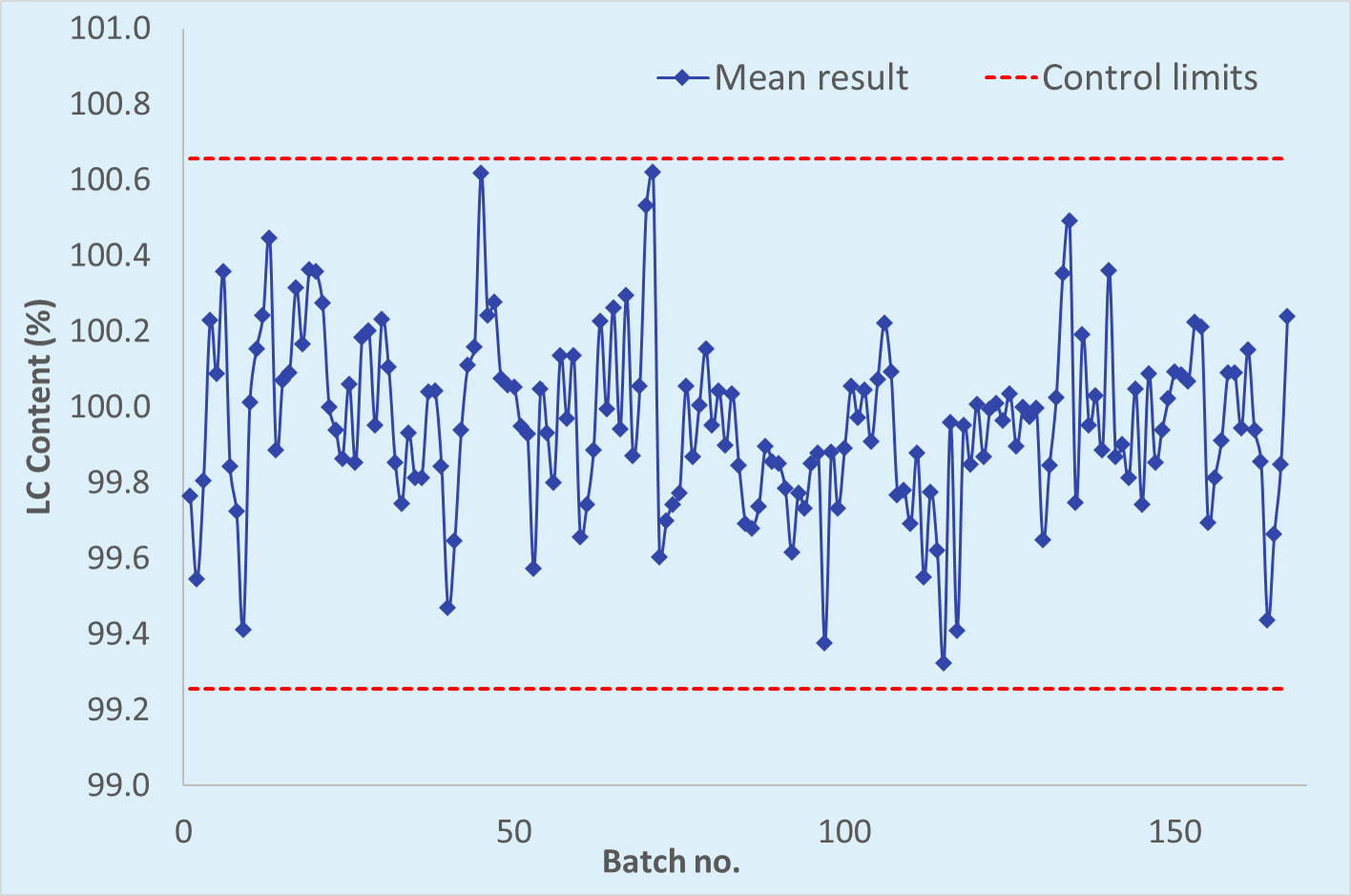
- Out-of-Specification (OOS) und Out-of-Trend (OOT) Untersuchungen,
Etablierung von Warngrenzen - Praktische Statistik
- Referenzstandards
- Stabilitätsuntersuchungen inkl. Stress-Stabilitäten (ANVISA)
- Validierung in der pharmazeutischen Analytik
- Verifizierung von Arzneibuchmethoden
- Transfer von Prüfverfahren
- Aufbau und Implementierung bzw. Überprüfung oder Audit von Qualitätssystemen zu o.g. Aspekten
Auf Ihre Schwerpunkte stelle ich mich gerne flexibel ein, sei es bei Planung oder Review von analytischen Untersuchungen, der Ableitung von geeigneten Akzeptanzkriterien, statistischen Berechnungen, der Bewertung der analytischen Ergebnisse, oder der Erstellung / Review von Berichten. Auf diese Weise können Sie von meiner langjährigen Experten– und Leitungstätigkeit in der pharmazeutischen Analytik und Qualitätskontrolle sowie in verschiedenen, auch internationalen Arbeitsgruppen profitieren.
Wenn ich Ihr Interesse geweckt habe, oder Sie sich zu weiteren Details informieren möchten, zögern Sie bitte nicht, mich zu kontaktieren:
+49 151 / 28 76 11 66